ТИРОНЕТ – все о щитовидной железе Для специалистов Журнал Тиронет 2011 год № 1
Клинические рекомендации по диагностике и лечению узлового зоба
Махмуд Хариб,
Хоссейн Хариб.
Перевод В.В. Фадеева
Клинический случай 2: кистозный узловой зоб
Мужчина 64 лет на протяжении последней недели предъявляет жалобы на боли в области шеи слева. Он отрицает травмы, повышение температуры, симптомы тиреотоксикоза; заболевания щитовидной железы в анамнезе отсутствуют. Симптомы нарушения функции щитовидной железы отсутствуют. С левой стороны пальпируется плотное образование щитовидной железы размером около 3 см; правая доля не изменена. ТТГ – 2,2 мЕд/л, св. Т4 – 1,5 мг/дл. При УЗИ выявлен узел размером 3,0×3,5×4,0 см, преимущественно кистозный, с небольшим тканевым компонентом (рис. 2). При ТАБ было получено 12 мл чистой желтоватой жидкости, в которой не было клеток. Но пункция под контролем УЗИ тканевого компонента выявила доброкачественный коллоидный зоб.
Как часто встречаются кистозные узлы?
По имеющимся данным около 25% солитарных узловых образований являются кистозными или имеют кистозный компонент [3]. Такие узлы могут быть полностью кистозными или смешанными кистозно-солидными. Истинные кисты в ЩЖ практически не встречаются и всегда доброкачественны. Поскольку кистозные узлы почти всегда доброкачественны, наличие кистозного компонента должно обнадеживать, тем не менее ТАБ для исключения опухолевого процесса проводить необходимо.
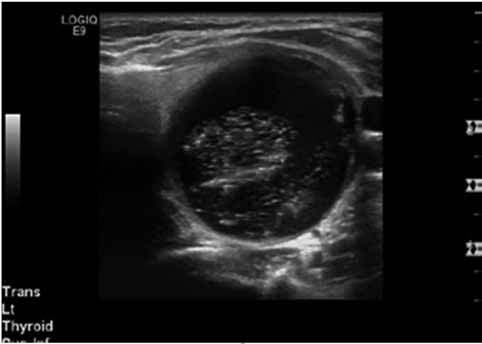 Рис. 2. Клинический случай 2. При УЗИ выявлен кистозный узел со взвесью в полости около задней стенки. При ТАБ получены данные о доброкачественном коллоидном узле
Рис. 2. Клинический случай 2. При УЗИ выявлен кистозный узел со взвесью в полости около задней стенки. При ТАБ получены данные о доброкачественном коллоидном узле
Каковы дальнейшие действия?
При бессимптомных мелких кистозных узлах показано динамическое наблюдение пациента. В большинстве случаев их размер особо не меняется, в связи с чем какиелибо активные действия показаны редко. При ТАБ кистозных узлов проводится аспирация их содержимого и эвакуированная жидкость направляется на анализ в лабораторию. В большинстве случаев это прозрачная желтоватая жидкость. Бесцветная жидкость часто происходит из околощитовидной железы и в этом случае целесообразна оценка уровня кальция и паратгормона. Геморрагическая жидкость с высокой вероятностью свидетельствует о злокачественности [22, 28]. После эвакуации жидкости необходимо под контролем УЗИ спунктировать солидный тканевой компонент узла. После дренирования кисты жидкость часто снова накапливается, порой с ещё большим увеличением размера, что может обусловить дискомфорт в области шеи и беспокойство пациента. В связи с этим лечение крупных кистозных узлов, обусловливающих компрессионные симптомы, нередко заканчивается оперативным вмешательством.
Альтернативой по отношению к хирургическому лечению кистозных узлов в тех ситуациях, когда для него есть показания, являются чрескожные инъекции этанола (ЧИЭ). Ряд итальянских исследований показал, что эффективность ЧИЭ при кистозных узлах составляет от 50 до 90% [29–34]. Вероятность рецидива псевдокист после ЧИЭ составляет менее 5%, а смешанных узлов с кистозным компонентом значительно больше – более 75%. Обычно одной инъекции оказывается достаточно для полного исчезновения или как минимум значительной редукции размера кисты; реже возникает необходимость в двух и более инъекциях этанола. Если ЧИЭ делается опытным специалистом, это безопасная процедура, не несущая стойких осложнений. ЧИЭ – минимально-инвазивная нехирургическая процедура, которая рекомендуется пациентам с доброкачественными кистозными узлами, которые вызывают локальные компрессионные симптомы. Предпринимались попытки использовать ЧИЭ для лечения солидных и «горячих» узлов, но в настоящее время для таких ситуаций этот метод использовать не рекомендуется [35].
Клинический случай 3: подозрительный узел
Женщина 46 лет, в правой доле ЩЖ обнаружено узловое образование, направлена к эндокринологу. Заболевания ЩЖ в анамнезе отсутствуют, как и облучение области головы и шеи в детстве. Локальные симптомы и симптомы нарушения функции ЩЖ отсутствуют. При пальпации ЩЖ в правой доле определяется солитарный узел размером 3×2 см, левая доля не изменена. Уровень ТТГ – 0,8 мЕд/л. При ТАБ в мазке отсутствует коллоид, повышена клеточность, формируются микрофолликулы. Сделано заключение о фолликулярной неоплазии.
Каков риск рака в данном случае?
По имеющимся данным риск рака в данном случае составляет около 10% [21, 25, 36]. В настоящее время отсутствуют морфологические критерии, которые бы позволили при фолликулярной неоплазии дифференцировать аденому от рака ЩЖ. Повторная биопсия, а также использование для неё толстых игл не рекомендуется, поскольку эти действия не привносят клинически значимой информации, которая позволит принять решение.
Эффективно ли использование молекулярных маркеров?
В качестве маркеров, которые могли бы использоваться при цитологическом исследовании для дифференциальной диагностики доброкачественных и злокачественных изменений, изучались многие молекулы. Наиболее известны BRAF, PAX-8, галектин-3, HBME и RET/PTC [37–40], при этом для части из них выпускаются коммерческие наборы. Тем не менее точность и предсказательная ценность этих тестов значительно варьируют и зачастую разнонаправленны. Пунктаты, позитивные по галектину-3, наиболее вероятно злокачественны [38]. В связи со сказанным в последних рекомендациях значится, что «рутинное использование молекулярных маркеров в клинической практике не рекомендуется и должно быть ограничено отдельными случаями» [1].
Каковы действия при фолликулярной неоплазии?
Принятая цитологическая классификация выделяет 4 категории заключений: неинформативное, доброкачественное, промежуточное и злокачественное [22, 35]. Рекомендации 2010 года выделяют 5 категорий, разделяя промежуточный вариант заключения на фолликулярную неоплазию (низкий риск) и подозрительный результат (высокий риск) (табл. 3). Всем пациентам с промежуточным цитологическим заключением показано хирургическое лечение, при этом объем оперативного лечения остается дискутабельным.
Последние рекомендации предлагают его определять в зависимости от варианта цитологического заключения. Если выявлена фолликулярная неоплазия, показано проведение лобэктомии с удалением перешейка, поскольку риск рака в этом случае достаточно низок (10%). Если заключение формулируется как подозрительное, более оптимально проведение тиреоидэктомии, поскольку риск рака достаточно высок (около 60%), особенно если у пациента в анамнезе было облучение шеи или во время операции определяются измененные шейные лимфоузлы. По данным большинства центров, интраоперационное изучение замороженных срезов имеет ограниченное значение для дифференциальной диагностики злокачественных и доброкачественных опухолей [21, 25].
Невозможность дифференцировать по данным ТАБ злокачественные и доброкачественные неоплазии, заложена в саму методологию цитологического исследования и приводит к большому числу потенциально ненужных операций, которых на сегодняшний день избежать невозможно.




